În primul rând, neacceptarea ideii că un corp uman este un “obiect” radiant, un “obiect” care în jurul său are un câmp electromagnetic, deşi este acceptată ideea că impulsurile nervoase sunt de tip electric, face ca metodele de investigare de tip captor de informaţie din aceste câmpuri, să nu fie considerate ca relevante. Pe lângă acestea mai există şi metodele bazate pe radiaţia infraroşie a organismului, ori pe captarea “zgomotului cuantic” al organismului în dinamicitate.
O primă întrebare care a apărut a fost care este compoziţia stelelor îndepărtate. De exemplu, se ştie cum sunt determinate elementele chimice din compoziţia Soarelui?
Una din principalele tehnici folosite este analiza spectrală. Această tehnică îşi are începuturile în 1750 când oamenii de ştiinţă au început să studieze comportamentul diferitelor substanţe în foc şi descompunerea luminii rezultate prin folosirea unei prisme. Astfel s-a descoperit că gazele fierbinţi degajate prin arderea materialelor emit lumină de diferite culori, adică au asociat un anumit spectru. Spectrul vizibil este reprezentat de radiaţiile luminoase cuprinse în intervalul 400÷750 nm obţinute în urma descărcărilor electrice în gaze sau ca urmare a radiaţiei termice a corpurilor incandescente. Ochiul omenesc este sensibil la această radiaţie, sensibilitatea maximă fiind situată în jur de 589 nm (puţin peste jumătatea intervalului). Această lungime de undă corespunde radiaţiei galbene. De exemplu, sarea gemă generează un spectru de lumină galben strălucitor (sarea e foarte importantă în conducerea energiei în organism, ajută la transportul substantelor nutritive spre celule, contribuie la echilibrul fluidelor în organism).
Mai mult, s-a observat că nu toate culorile curcubeului (ROGVAIV) apăreau în acest spectru, existând zone întunecate în cadrul acestuia. Există chiar materiale care emit doar câteva nuanţe din întregul spectru vizibil. Mult mai târziu, în 1820, s-a stabilit clar că studierea acestui spectru de emisie reprezenta o modalitate foarte bună de a detecta şi identifica mici cantităţi dintr-un element aflat în compoziţia unei pulberi încălzite la o flacără.
Studiile luminii solare au dus la descoperirea unui spectru cu mici "goluri" vizibile sub forma unor foarte subţiri linii întunecate prezente printre culorile curcubeului. Următoarele întrebări care au apărut se refereau la cauza existentei liniilor spectrale specifice fiecărei substanţe şi relaţia dintre acestea şi compoziţia substanţelor.
Sfârşitul secolului XIX a adus răspunsuri dar şi noi semne de întrebare. Prin studiile efectuate în domeniul spectrului continuu de radiaţii emis de diferite substanţe solide încălzite s-a putut determina temperatura acestora.
Pe parcursul acestor experimente s-a observat şi că anumite obiecte absorb lumina extrem de eficient, fiind absorbante aproape ideale. Au fost numite corpuri absolut negre deoarece absorbeau aproape toată radiaţia electromagnetică incidentă pe suprafaţa lor. Temperatura unui corp absolut negru determină distribuţia culorilor sau lungimilor de undă ale luminii emise.
Un exemplu de corp negru este un cuptor în interiorul căruia radiaţiile electromagnetice (lumină şi căldură) există sub forma unor unde staţionare de culori sau lungimi de undă variabile. Aceste unde vibrează asemenea corzilor unei chitare fixate la ambele capete. La temperaturi scăzute, undele din interiorul cuptorului se situează în domeniul infraroşu al spectrului, invizibile pentru ochiul uman. Pe măsură ce temperatura creşte, cuptorul se încinge şi începe să radieze lumină roşie, iar dacă temperatura continuă să crească culoarea dominantă devine portocaliu, apoi galben şi mai târziu alb-albăstrui. Zona de intensitate maximă a energiei radiate se deplasează spre lungimi de undă mai mici odată cu creşterea temperaturii.
Fenomenul de „catastrofă” ultravioletă a reprezentat un moment cuantic deosebit în domeniul fizicii. S-a observat că pe măsură ce se înaintează în interiorul zonei ultraviolete a spectrului, este emisă tot mai puţină lumină. Aceste fenomen aparent inexplicabil a fost studiat cu mare interes de unul din pionierii fizicii cuantice. Max Planck este cel care a conştientizat faptul că energia putea fi emisă sau absorbită doar în valori discrete specifice fiecărei culori în parte. El a introdus noţiunea de cuantă (latină – cantitate discretă) pentru a cuantifica energia (E=h•ν, unde h=constanta lui Planck, ν =frecvenţa radiaţiei).
|
Concluzia lui Planck despre emisia energiei în mod discret a fost folosită de Albert Einstein în 1905 pentru a explica un alt fenomen care nu respecta legile fizicii clasice. S-a observat că iluminarea unei plăci metalice putea fi însoţită uneori de eliberarea de electroni de pe suprafaţa respectivă, numai că lungimea de undă a luminii folosite trebuia să atingă o anume valoare înainte de a fi dislocat măcar un electron. Acest fenomen este cunoscut sub denumirea de efect fotoelectric. În 1923, fizicianul Arthur Compton a reconfirmat teoria lui Einstein cînd a explicat acest efect. O aplicabilitate a zilelor noastre a efectului fotoelectric sunt panourile solare care transformă lumina (fotonii) în curent electric (electroni). |
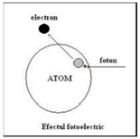 |
Se poate creşte oricât cantitatea (intensitatea) de lumină direcţionată spre placa metalică, dar dacă lumina nu are lungimea de undă (culoarea) corespunzătoare, electronii rămân în structura metalică. Einstein a concluzionat că lumina care atingea suprafaţa metalică există sub forma unor pachete discrete şi până un singur "pachet" de lumină nu avea suficientă energie pentru a disloca un electron, acesta din urmă rămânea captiv în structura metalică. Şi, aşa cum sugerase şi Planck, lungimea de undă şi frecvenţa asociate luminii folosite, sunt măsura cantităţii de energie conţinută în fie-care pachet, sau cuantă, din această lumină.
Aşa că în timp ce cuantele de lumină albastră au suficientă energie pentru a elibera un electron, cuantele de lumină roşie nu puteau face acest lucru, oricât de multe ar fi lovit placa metalică.
Acest comportament sugerează ideea că lumina este o particulă şi nu o undă, numai că există fenomene care indică faptul că lumina are un caracter ondulatoriu: difracţia, refracţia, interferenţa luminii, etc. Deci lumina este şi particulă şi undă.
Aceste "pachete" sau cuante de lumină extrem de mici au fost numite fotoni (de la grecescul photos -care înseamnă tocmai lumină).
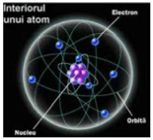 |
Explicarea fenomenelor legate de atomi şi fotoni a început tot în primele decenii ale secolului XIX. Neils Bohr propune primul model atomic funcţional al atomului de hidrogen. În cadrul acestui model, electronul orbitează în jurul nucleului (mişcare orbitală) asemenea planetelor în jurul Soarelui. Folosind ideea cuantificării energiei introdusă de Planck pentru explicarea catastrofei ultraviolete, Bohr afirmă că în mişcarea sa în interiorul atomului de hidrogen electronul poate avea doar valori discrete ale momentului cinetic atunci când orbitează în jurul nucleului, adică poate orbita doar la anumite distanţe de acesta. În interiorul unui atom electronii emit radiaţie electromagnetică doar atunci când "sar" de pe o orbită permisă pe o alta, iar energia radiaţiei emise ne oferă informaţii despre orbitele permise. |
 |
Datorită concentrării şi intuiţiei sale, N. Bohr a creat un model extraordinar al atomului de hidrogen, care explică detaliat spectrul atomic al acestui element. Explicarea orbitelor electronice ale hidrogenului a fost posibilă datorită abordării concepţiei cuantice. În 1924, Louis de Broglie avansa o idee simplă şi curajoasă pentru înţelegerea lumii atomilor, care de asemenea a reprezentat un adevărat salt cuantic. Din moment ce Einstein, Planck şi Compton stabiliseră clar faptul că lumina prezenta caracteristici duale, de corpuscul şi de undă, Louis de Broglie sugerează că şi materia (protoni, electroni, atomi, obiecte macroscopice) e posibil să se comporte uneori asemenea undelor. |
Plecând de la imprecizia poziţiei electronilor în cadrul orbitelor undelor staţionare ale lui de Broglie, Werner Heisenberg introduce o idee extraordinară pe care o formulează în felul următor: “Pe măsură ce determinăm mai precis poziţia unui electron, precizia de determinare a vitezei sale scade şi viceversa.” Aceasta este una din formele celebrului principiu al incertitudinii.
Şi deşi fraza anterioară sună destul de straniu, ea conţine conceptul necesar înţelegerii naturii duale, particulă-undă, a obiectelor din lumea cuantică. Acest enunţ al lui Heisenberg a condus la înţelegerea faptului că particulele subatomice pot dispărea pentru a reapărea într-o altă poziţie în spaţiu. Şi pot face asta fără a exista în spaţiul dintre cele două puncte. Extraordinar, nu-i așa?
Când un electron este parte a unui atom, locurile de unde poate dispărea şi cele în care poate reapărea sunt doar anumite zone din jurul nucleului. Şi asta creează aparenţa unui "înveliş", aşa-zisul orbital electronic. Particulele elementare pot exista, de asemeni, în mai mult de o locaţie în acelaşi timp, cu condiţia ca timpul să fie extrem de scurt. Un electron poate călători dintr-un loc în altul parcurgând toate drumurile posibile simultan. Şi, încă mai şocant, aceste particule pot apărea din nimic, pentru a exista pentru un timp foarte scurt şi a dispărea, la fel, în neant.
Oamenii de ştiinţă le-au numit particule virtuale. Deşi virtuale, ele generează efecte "foarte" reale. Toate aceste manifestări uimitoare fac ca descrierea particulelor subatomice să fie extrem de dificilă şi inexactă, dar existenţa însăşi este inexactă la această scară cuantică.
Particula "oscilează" parcă încontinuu între două lumi, apărând şi dispărând, iar acele locuri în care valorile undei asociate sunt maxime sunt cele unde particula se materializează de cele mai multe ori, în timp ce locaţiile unde valorile undei asociate sunt minime sunt cele pe care particula le evită. Unda este o veritabilă hartă a existenţei particulei şi, pe măsură ce unda se modifică, particula se schimbă la rândul ei. Aceste teorii explică foarte bine modificările grafice prezente la generatorul cuantic nonlinear Metatron (linia roşie – semnal de intrare şi linia albastră – semnal de ieşire). Cele două linii nu pot fi interpretate şi nu au sens decât împreună, la fel ca şi particula şi unda asociată.
Enunţul lui Werner Heisenberg conţine mai mult decât o simplă analiză calitativă, atunci când face referire la imposibilitatea cunoaşterii simultane a poziţiei şi vitezei (mai exact impulsului, dat de produsul dintre viteză şi masă) unei particule. Germanul a scris şi o ecuaţie care descrie cantitativ relaţia dintre cei doi indicatori. Această informaţie ajută la o mai uşoară înţelegere a atomului de hidrogen, descris extrem de detaliat cu ajutorul ecuaţiei lui Schrödinger.
Erwin Schrödinger a dezvoltat o ecuaţie care să descrie corect mişcarea şi comportamentul "locuitorilor" lumii cuantice. Dacă Bohr şi de Broglie reuşiseră să descrie corect atomul de hidrogen, ecuaţia lui Schrödinger făcea şi ea acest lucru. Această ecuaţie explică nu numai comportamentul hidrogenului, dar descrie nici mai mult nici mai puţin decât atomii tuturor elementelor din Univers.
Mecanica cuantică a lui Schrödinger explică comportamentul tuturor elementelor din Tabelul Periodic. Soluţia acestei ecuaţii, numită “funcţie de undă”, descrie cu o acurateţe fantastică lumea în care trăim.
Atomul nu este întotdeauna în starea de energie minimă. Aşa cum există mai multe orbite permise în cadrul modelului atomic al lui Bohr, există şi alte niveluri energetice în cadrul modelului cuantic al atomului de hidrogen. Aceste stări sunt definite în principal prin intermediul numărului cuantic “n” de care am vorbit mai sus. Şi pentru fiecare stare electronul posedă energii diferite care rezultă din forma orbitalului electronic. Orbitalul poate avea formă simetrică (aceeaşi în toate direcţiile) sau combinaţii de forme (halteră, o sferă în interiorul alteia etc.).
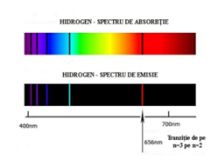
Un electron aflat pe cel mai de jos nivel energetic într-un atom poate sa intre în contact şi să absoarbă energia unui foton, primind astfel energie suficientă pentru a sări pe următorul nivel. Iar în cadrul procesului invers electronul revine pe nivelul energetic anterior, proces însoţit de eliberarea unui foton. Culoarea fotonului depinde de diferenţa de energie dintre cele două orbitaluri.
Astfel se explică apariţia liniilor spectrale asociate fiecărui element chimic. Din moment ce lumina albă are în componenţă toate culorile spectrului, atunci când un fascicul de lumină albă acţionează asupra unei mostre dintr-un element chimic în condiţii corespunzătoare, atomii acestuia absorb toţi fotonii care le permit electronilor lor să efectueze salturi între orbitali.
Teoria cuantumului entropic este o parte esenţială a teoriei informaţionale dezvoltată în anii '80 de Theodore van Hoven (1922-1995). Th. van Hoven consideră informaţia o categorie materială care ne arată nivelul de organizare a structurii interne a unui obiect şi e corelată cu caracteristicile de bază (energia şi masa obiectului) [60]. Câmpul cuantic entropic reprezintă un cvasicâmp generat prin producerea deformării spaţio-temporale.
Analiza a doi electroni alăturati dezvăluie aspecte diferite din perspectiva abordării cuantice. În mod normal, când două lucruri sunt identice, le privim ca pe nişte entităţi independente. Atâta vreme cât putem să le monitorizăm atent, le putem trata în mod separat şi le putem identifica astfel: A şi B, ori X şi Y, sau 1 şi 2. De unde apare diferenţa în cazul unui sistem cuantic format din 2 electroni, fie că aceştia sunt parte a unui atom sau nu? Din moment ce aceştia apar şi dispar în mod constant, existând parcă la graniţa dintre 2 lumi, şi deoarece sunt absolut identici, este imposibil ca unul dintre ei să fie constant localizat.
Din această cauză trebuie să folosim o funcţie de undă combinată pentru a descrie perechea formată din cei doi electroni, neputând folosi două funcţii de undă independente. Această nouă funcţie de undă asociată celor două particule va avea două părţi componente. Iar aceste două părţi fie se vor însuma una cu alta, fie se vor scădea una din cealaltă. Fizicienii spun că aceste operaţii vor genera o funcţie de undă fie simetrică, fie antisimetrică.
S-a constatat că doar funcţia de undă antisimetrică poate fi aplicată în cazul electronilor. Este şi cazul quarcurilor, al protonilor şi al neutronilor. Dacă electronii sunt în aceeaşi stare, atunci aceste două unde vor fi una imaginea în oglindă a celeilalte. Pe măsură ce valoarea uneia creşte, valoarea celeilalte descreşte perfect sincronizat cu creşterea celei dintâi. Combinate, aceste două unde se anulează reciproc. Şi din moment ce unda este o hartă a poziţiei electronilor, asta înseamnă că lipsa undei implică lipsa electronilor! Rezultă de aici că doi electroni nu pot exista în aceeaşi stare cuantică deoarece asta ar face ca funcţia lor combinată de undă să devină nulă.
Componentele care concură la "starea cuantică" a unui electron într-un atom sunt orbitalul pe care îl ocupă şi o altă proprietate asociată electronului numită “spin”. Putem face o paralelă între un titirez şi un electron pentru a înţelege ce este "spinul" acestuia. Mişcarea de spin este mişcarea de rotaţie a electronului în jurul axei sale. Un electron poate avea spin de dreapta şi spin de stânga. Astfel numai 2 electroni pot ocupa acelaşi orbital într-un atom, având obligatoriu valori diferite şi opuse ale spinului. Ceilalţi electroni din structura atomului trebuie să ocupe orbitalurile de energii superioare. Această regulă se numeşte “Principiul excluziunii” şi a fost formulată de către fizicianul austriac Wolfgang Pauli. Dacă acest principiu nu ar fi respectat, toţi electronii ar exista pe orbitalul cu cea mai mică energie, atomii s-ar comporta complet diferit şi, în consecinţă, Universul ar fi un loc cu totul diferit!
Proprietatea numită “spin”este cuantificabilă şi din această cauză, particulele fundamentale pot fi clasificate în două familii distincte. Enrico Fermi şi Satyendra Bose sunt fizicienii care au dat nume celor două familii diferite de particule.
Particulele care au "spinul" egal cu 1/2, 3/2, 5/2 ş.a.m.d. aparţin familiei "fermionilor". Fizicianul italian Enrico Fermi împreună cu Paul Dirac au dezvoltat o metodă statistică pentru a le descrie proprietăţile. Se spune că fermionii au spin semi- întreg. Electronii, quarcurile, protonii şi neutronii fac cu toţii parte din această familie.
Particulele fundamentale din cealaltă familie au valori ale "spinului" egale cu 0,1,2,3 etc. Se cheamă "bosoni", după numele lui Satyendra Bose care împreună cu Albert Einstein a dezvoltat o metodă statistică pentru a descrie această familie. Se spune că bosonii au spin întreg. Spre deosebire de fermioni, bosonii nu se supun principiului excluziunii. Grupuri de foarte mulţi bosoni există pe cel mai scăzut nivel energetic disponibil. Fotonii, gluonii şi, teoretic, gravitonii, sunt parte a acestei familii. Dacă bosonii ar fi respectat principiul excluziunii, multe din marile invenţii tehnologice moderne nu ar fi existat. Este şi cazul laserilor, al căror principiu de funcţionare necesită existenţa unui număr imens de fotoni în aceeaşi stare simultan.
Toate noţiunile noi despre dualitate, particule virtuale, excluziune şi incertitudine apartin domeniului cuantic. Tot în această zonă sunt incluse fenomenul de inseparabilitate cuantică şi colapsul funcţiei de undă asociat acestui fenomen.
Fenomenul de inseparabilitate cuantică apare atunci când două sau mai multe particule interacţionează, funcţiile lor de undă se combină de o asemenea manieră că anumite proprietăţi ale fiecăreia depind de ceea ce se petrece cu cealaltă. Dacă ulterior particulele sunt separate cu atenţie şi ţinute izolat în locaţii îndepărtate, ele continuă să existe ca o pereche atâta vreme cât nu sunt deranjate, cu proprietăţile uneia depinzând de ale celeilalte.
Când asupra uneia dintre particule intervine un observator uman în vederea măsurării anumitor proprietăţi ale sale, funcţia de undă "se prăbuşeşte" instantaneu. Fizicienii numesc acest fenomen "colapsul funcţiei de undă". Instantaneu, proprietăţile interdependente ale celeilalte particule iau şi ele valorile corespunzătoare. De exemplu, putem construi un dispozitiv care să emită perechi de electroni cu valori ale spinului opuse şi interdependente. Nici unul dintre electroni nu are o valoare fixă a spinului, ambii oscilând între spin orientat în sus şi în jos. Dar funcţiile lor de undă depind cumva una de cealaltă astfel că de fiecare dată când se acţionează asupra unuia dintre electroni, acesta orientându-şi spinul - să zicem - în sus, atunci instantaneu spinul celuilalt electron se fixează în starea opusă (în jos).
Acest colaps instantaneu are loc şi atunci când cei doi electroni sunt dispuşi unul lângă altul, dar şi dacă particulele se găsesc la mii de kilometri distanţă una de cealaltă.
Deşi acest comportament este straniu, se întrevăd o mulţime de aplicaţii ale acestui fenomen în tehnologii moderne precum computerele cuantice, criptografiacuantică sau teleportarea cuantică. Datorită faptului că o mulţime de cercetări se desfăşoară în aceste domenii, mulţi oameni de ştiinţă nu au nici cea mai mică îndoială cu privire la validitatea acestor observaţii bizare.
Inseparabilitatea cuantică a fost testată de multe ori, ajungându-se chiar la experimente în cadrul cărora particulele au fost izolate la distanţe de peste 100 de kilometri, ceea ce dovedeşte că fenomenul persistă chiar dacă distanţa între particulele atât de misterios conectate creşte.
Se poate face o paralelă între, pe de o parte, conceptele de continuitate şi discontinuitate (linear şi nonlinear) aşa cum reies acestea din perspectiva fizicii clasice, respectiv cuantice şi, pe de altă parte, ideile de analogic şi digital, atât de utilizate în tehnologiile moderne. Astfel, continuu este echivalent cu analogic, iar dacă se vorbește de discontinuitate, se face referire la ceva digital.
Tendinţa actuală în tehnologiile audio, video şi de comunicaţii este „trecerea la digital”. În locul unei palete continue de culori pentru dispozitivele video, ne limităm la un număr finit de nuanţe. În locul unei imagini clasice, fotografiile de astăzi sunt împărţite în pixeli.
Şi aceasta seamănă foarte mult cu felul în care Universul nostru funcţionează la scară microscopică. Întreg Universul "a trecut la digital" înainte cu 14 miliarde de ani ca cineva să se fi gândit la aşa ceva! Spaţiul, timpul, energia, momentul cinetic, toate sunt digitale, discontinue, nonlineare. Doar anumite valori sunt permise, iar acest caracter discontinuu este descris cu precizie de mecanica cuantică. Toate aceste notiuni şi teorii de fizică cuantică poate par dificil de înţeles şi abstracte la o primă citire, dar valoarea lor teoretică şi aplicabilitatea practică sunt revoluţionare. Fără aceste deducţii intuitive geniale ale unor oameni de ştiinţă uimitori, progresul ar fi fost mult mai încetinit. Metoda de analiză nonlineară are la bază toate aceste noţiuni de fizică cuantică şi a găsit aplicabilitate în domeniul sănătăţii.
Cititi mai mult...